Forfatter:
Lewis Jackson
Oprettelsesdato:
12 Kan 2021
Opdateringsdato:
1 Juli 2024
Indhold
At bestemme antallet af neutroner i et atom er ret simpelt, du behøver ikke engang at lave nogen eksperimenter. For at beregne antallet af neutroner i et normalt atom eller en isotop skal du bare have et periodisk system klar og følge instruktionerne.
Trin
Metode 1 af 2: Find antallet af neutroner i et normalt atom
Bestem elementets placering på det periodiske system. For eksempel finder vi elementet osmium (Os) i den sjette række fra toppen.
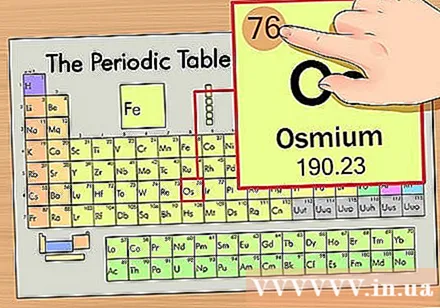
Find elementets atomnummer. Dette er det mest iøjnefaldende tal, der går efter hvert element og ligger over hovedsymbolet (på tavlen, vi bruger, er der ingen andre tal). Atomnummer er antallet af protoner i et enkelt atom af dette element. Os er tallet 76, hvilket betyder, at der er 76 protoner i et osmiumatom.- Antallet af protoner ændres aldrig i et element; det er i det væsentlige det definerende kendetegn ved et element.
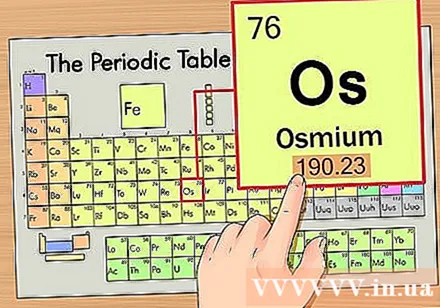
Find elementets atomvægt. Dette tal findes normalt under det primære symbol. Bemærk, at det periodiske system i dette eksempel kun har atomnummer og ingen atomvægt. Ikke alle periodiske tabeller. Osmium har en atomvægt på 190,23.
Rund atomvægten til nærmeste heltal for at få atommassen. For eksempel ville 190,23 blive afrundet til 190, så osmiumets atommasse er 190.- Atomvægt er den gennemsnitlige værdi af isotoper af det samme kemiske element, hvorfor det normalt ikke er et heltal.
Træk atomnummeret fra atommassen. Da det meste af atommassen er massen af protoner og neutroner, trækker du antallet af protoner fra atommassen (dvs. atomnummer) vil du tælle få antallet af neutroner i atomet. Tallet efter decimal repræsenterer den meget lille masse af elektroner i atomet. I dette eksempel har vi: 190 (masseatom) - 76 (antal protoner) = 114 (antal neutroner).
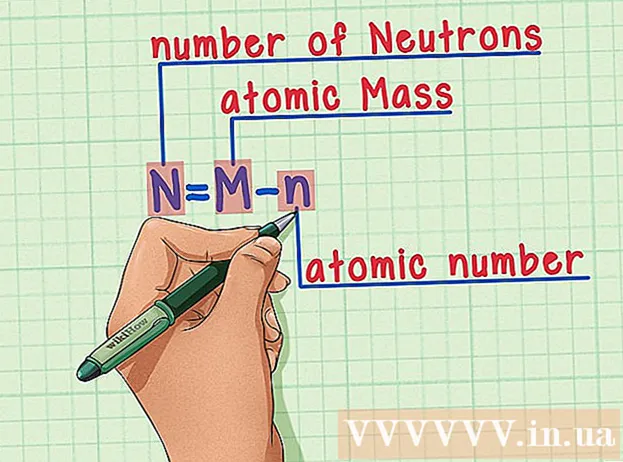
Husk opskriften udenad. For at finde antallet af neutroner anvender vi blot følgende formel: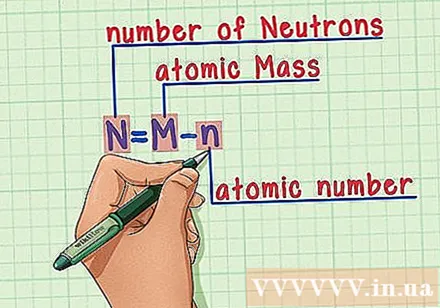
- N = M - n
- N = antal neutroner
- M = atommasse
- n = atomnummer
- N = M - n
Metode 2 af 2: Find antallet af neutroner i isotopen
Bestem elementets placering på det periodiske system. Lad os tage elementet carbon-14 isotop som et eksempel. Da isotopformen af kulstof-14 simpelthen er kulstof (C), skal du kigge efter kulstof i det periodiske system (anden række fra toppen).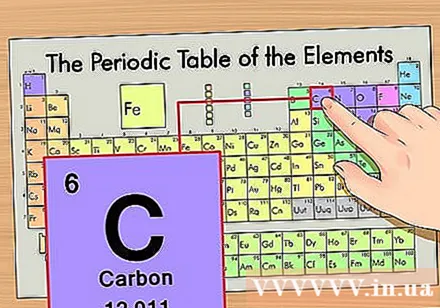
Find elementets atomnummer. Dette er det mest iøjnefaldende tal, der går efter hvert element og ligger over hovedsymbolet (på tavlen, vi bruger, er der ingen andre tal). Atomnummer er antallet af protoner i et enkelt atom af dette element. C er nummer 6, hvilket betyder, at der er 6 protoner i et carbonatom.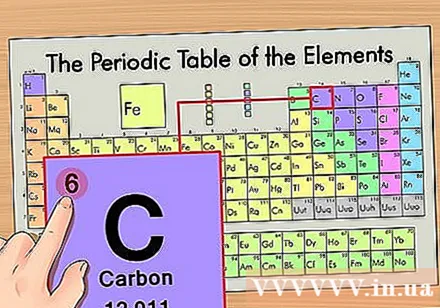
Find atommasse. Dette er ekstremt let med isotoper, fordi de er opkaldt efter atommasse. For eksempel ville carbon-14 have en atommasse på 14. Når du først har fundet atommassen af isotopen, vil de resterende trin til at finde antallet af neutroner være de samme som for et normalt atom.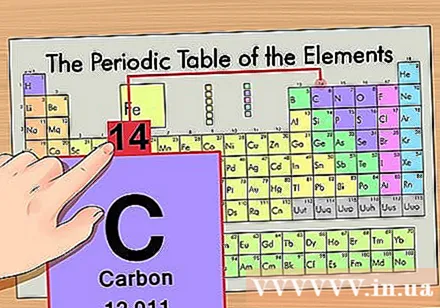
Træk atomnummeret fra atommassen. Da det meste af atommassen er massen af protoner og neutroner, trækker du antallet af protoner fra atommassen (dvs. atomnummer) vil du tælle få antallet af neutroner i atomet. Tallet efter decimal repræsenterer den meget lille masse af elektroner i atomet. I dette eksempel har vi: 14 (masseatom) - 6 (antal protoner) = 8 (antal neutroner).
Husk opskriften udenad. For at finde antallet af neutroner anvender vi følgende formel: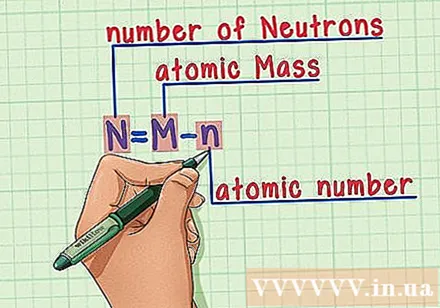
- N = M - n
- N = antal neutroner
- M = atommasse
- n = atomnummer
- N = M - n
Råd
- Massen af et element er stort set massen af protoner og neutroner, mens masserne af elektroner og andre elementer er ubetydelige (tæt på nul). Da massen af protonen er omtrent lig med massen af neutronen, og atomnummeret repræsenterer antallet af protoner, behøver vi kun at trække antallet af protoner fra den samlede masse.
- Hvis du ikke kan huske betydningen af tallene i det periodiske system, skal du huske at det periodiske system normalt er bygget på atomnumre (dvs. antallet af protoner), der starter ved 1 (brint) og inkrementerer en enhed fra fra venstre mod højre og slutter med 118 (ununoctium). Da antallet af protoner er et identificerende træk ved hvert atom, er det den enkleste egenskab, hvorpå elementerne er arrangeret. (For eksempel er et atom med 2 protoner altid helium, ligesom et atom med 79 protoner altid er guld.)
Kilder og citater
- Interaktivt periodisk system